锌焙砂浸出
一、实验目的
1、掌握锌焙砂浸出过程的基本原理。
2、学习φ-pH图在湿法浸出过程中的运用。
二、实验原理
硫化锌精矿经氧化焙烧后,锌在焙砂中以ZnO、ZnSO4、ZnS、ZnO·SiO2、ZnO·Fe2O3、ZnO·Al2O3等形态存在。
锌焙砂的浸出过程是指用硫酸水溶液(或废电解液)做溶剂,将锌焙砂中的锌溶液溶解转入溶液的过程,其反应为:
ZnO+H2SO4=ZnSO4+H2O (1)
浸出的目的是尽可能完全和迅速的把锌焙砂中的锌转入溶液,同时使其与杂质分离。实际上ZnO、ZnSO4和ZnO·SiO2很容易进入稀硫酸水溶液中;而ZnS则总溶于热浓硫酸中;而ZnO·Fe2O3和ZnO·Al2O3则溶解很少,进入浸出残渣中。问题在于锌浸出的同时,相当数量的杂质(Cu、Cd、Fe、As、Sd等)也转入溶液,为减少杂质的进入,工业上将浸出分为中性浸出和酸性浸出,中性浸出除需把锌浸出外,还承担着中和水解净化除去Fe、As、Cd等杂质的任务,在保证浸出液质量的同时,最大限度的溶出锌。中性浸出工业实践中,溶液中锌的水解析出的pH值与其浓度有关,溶液中锌浓度与锌水解沉淀析出的pH值关系图2-1。
实践中,中性浸出的pH值控制在5~5.2。酸性浸出除考虑杂质少量溶解外,重要的是使锌更多的溶解,以提高焙砂中锌的浸出率,其终点酸度一般控制在1~5g/l H2SO4。
杂质离子与锌分离最简单的方法是中和水解沉淀。其原理可用φ-pH图(2-1)来分析。从图2-1可看出:Fe2+水解沉淀的pH值大于Zn2+的水解pH值,而Fe3+水解沉淀的pH值则比Zn2+水解pH值小得多,在保证浸出液中ZnSO4不发生水解沉淀情况下,用中和水解沉淀法只能将Fe3+有效的除去,为了净化除铁,则必须将溶液中的Fe2+氧化成Fe3+,在工业生产中一般用软锰矿进行氧化,本试验用过氧化氢作氧化剂。其反应如下:
2FeSO4+H2O2+H2SO4=Fe2(SO4)3+2H2O (2)
所得到的三价铁的硫酸盐按下式水解:
Fe2(SO4)3++6H2O=2Fe(OH)3+H2SO4 (3)
反应产生的硫酸采用家焙砂和石灰乳中和,本试验采用Na2CO3溶液中和。
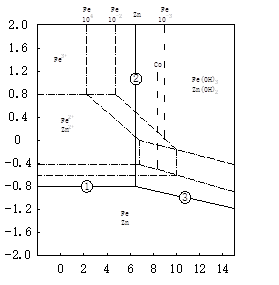
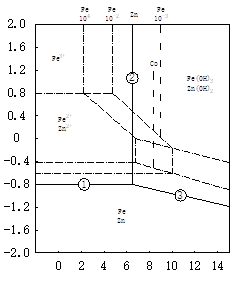
图1-1 溶液中锌浓度与氢氧化 图1-2 锌焙烧砂中性浸出原理
锌开始沉淀析出的PH值
三、实验设备、试剂及实验技术条件
1、实验设备
(1)磁力子搅拌器 1台;
(2)浸出容器及配件 1套;
(3)分析仪器 1套;
(4)锌焙砂;
(5)工业硫酸;
(6)饱和Na2CO3液;
(7)过氧化氢。
2、实验技术条件
(1)浸出技术条件
温 度: 60~70℃
硫酸液: 含H2SO4:110g/l;
液固比: 8∶1;
时 间: 30分钟;
搅 拌: 磁力搅拌;
锌焙砂: 40g。
(2)中和技术条件
温 度: 40~50℃;
搅 拌: 磁力搅拌;
起始氧化剂:过氧化氢;
中和剂: 饱和Na2CO3液;
pH值终点: 5.2~5.4。
四、工艺流程及操作步骤
(一)工艺流程
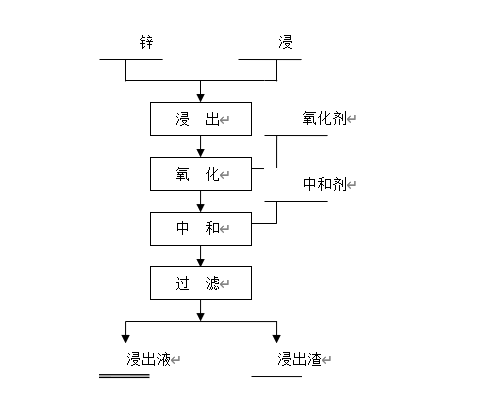
图2-3 锌浸出工艺流程
(二)操作步骤
(1)配制溶剂
根据工业硫酸的比重和浸出技术条件(锌焙砂、硫酸液浓度、液固比),在量筒中配制溶剂,配好的溶剂取样分析(分析方法见后)溶剂的含酸量(g/l),并将溶剂倒入浸出容器中,置于磁力加热搅拌器上进行加热。称取锌焙砂40克。
(2)浸出
当溶液温度升到60~70℃时,轻轻放入磁力子,开动搅拌器,控制在适当的转速后,缓慢加入锌焙砂,浸出即开始,维持技术条件30分钟。
(3)中和
浸出30分钟后,加入过氧化氢5ml,搅拌5~10分钟,随后缓慢加入饱和Na2CO3液中和,边中和边用pH试纸检测矿浆pH值达到5左右时,应更缓慢的加入饱和Na2CO3液,当pH值=5.2~5.4时,停止保温加热,停止搅拌,并注意观察沉渣及颗粒长大情况。
(4)过滤
矿浆经澄清后,用瓷漏斗真空过滤,滤渣经水洗2~3次后弃去,滤液用量筒量取体积,并记录,滤液倒入净化容器中留待分析和净化实验。
(5)浸出液含Zn量的测定
采用EDTA容量法(络合滴定)测定浸出液Zn含量,其分析步骤如下:
用移液管准确吸取浸出液1ml于300ml三角杯中,加蒸馏水20ml;加0.1%甲基橙1滴,加1∶1HCl中和甲基橙变红色;
加1∶1氨水2~3滴,使其变黄;
加醋酸—醋酸钠缓冲液10ml,加10%的硫代硫酸钠2~3ml混匀;
加0.5%二甲酚橙指示剂2滴,用EDTA标准溶液滴至溶液由酒红色变至亮黄色为终点。
浸出液含锌计算:

式中:G— 浸出液含锌总量(g);
V— 滴定消耗的EDTA量(ml);
T—滴定度(g/ml);
W—浸出液总体积(ml);
X—取来分析的浸出液的量(ml)。
(6)酸的测定
采用酸碱中和法测定溶剂的酸含量,分析步骤如下:
用移液管准确吸取浸出液1ml于300ml三角杯中,加蒸馏水30~50ml;
加0.1%甲基橙2~3滴,用标准氢氧化钠滴定至溶液由红色至黄色为终点。
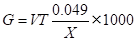
式中:G— 溶剂含酸量(g/l);
V— 滴定消耗的NaOH量(ml);
T— 滴定度(g/ml);
X— 取来分析的溶剂量(ml)。
五、实验记录
焙砂重量:(g); 焙砂含锌:(%);
浸出液体积:(ml); 浸出液含锌总量:(g)。
表1-1 实验记录
时 间 |
操作步骤 |
试剂用量 |
温 度 |
pH/(g/l) |
现 象 |
|
|
|
|
|
|
六、数据处理和报告编写
(1)浸出率计算

焙砂中总含Zn量=焙砂量×焙砂含Zn量%
(2)实验报告内容
1.简要叙述锌浸出的基本原理,工艺流程。
2.简述实验操作,评述浸出结果。
3.应采取哪些措施强化浸出结果,提高锌的浸出率,同时使杂质尽可能少转入溶液。
4.简述如何运用φ-pH图来控制工艺条件和锌焙砂中杂质在中性浸出时的去向。
5.谈谈你对本实验有何改进意见。